Что такое галогены? Химические элементы фтор, хлор, иод и астат. Галоген что такое
Галогены - это... Что такое Галогены?
| В этой статье не хватает ссылок на источники информации. Информация должна быть проверяема, иначе она может быть поставлена под сомнение и удалена. Вы можете отредактировать эту статью, добавив ссылки на авторитетные источники. Эта отметка установлена 14 декабря 2011. |
| ||||||
| ||||||
Галоге́ны (от греч. ἁλός — соль и γένος — рождение, происхождение; иногда употребляется устаревшее название гало́иды) — химические элементы 17-й группы периодической таблицы химических элементов Д.И. Менделеева (по устаревшей классификации — элементы главной подгруппы VII группы)[1].
Реагируют почти со всеми простыми веществами, кроме некоторых неметаллов. Все галогены — энергичные окислители, поэтому встречаются в природе только в виде соединений. С увеличением порядкового номера химическая активность галогенов уменьшается, химическая активность галогенид-ионов F−, Cl−, Br−, I−, At− уменьшается.
К галогенам относятся фтор F, хлор Cl, бром Br, иод I, астат At, а также (формально) искусственный элемент унунсептий Uus.
Все галогены — неметаллы. На внешнем энергетическом уровне 7 электронов, являются сильными окислителями. При взаимодействии с металлами возникает ионная связь, и образуются соли. Галогены, (кроме F) при взаимодействии с более электроотрицательными элементами, могут проявлять и восстановительные свойства вплоть до высшей степени окисления +7.
Распространённость элементов и получение простых веществ
Как уже было сказано выше, галогены имеют высокую реакционную способность, поэтому встречаются в природе обычно в виде соединений.
Их распространённость в земной коре уменьшается при увеличении атомного радиуса от фтора к иоду. Количество астата в земной коре измеряется граммами, а унунсептий в природе отсутствует. Фтор, хлор, бром и иод производятся в промышленных масштабах, причем хлор производится в гораздо больших количествах.
В природе эти элементы встречаются в основном в виде галогенидов (за исключением иода, который также встречается в виде иодата натрия или калия в месторождениях нитратов щелочных металлов). Поскольку многие хлориды, бромиды и иодиды растворимы в воде, то эти анионы присутствуют в океане и природных рассолах. Основным источником фтора является фторид кальция, который очень малорастворим и находится в осадочных породах (как флюорит CaF2).
Основным способом получения простых веществ является окисление галогенидов. Высокие положительные стандартные электродные потенциалы Eo(F2/F−) = +2,87 В и Eo(Cl2/Cl−) = +1,36 В показывают, что окислить ионы F− и Cl− можно только сильными окислителями. В промышленности применяется только электролитическое окисление. При получении фтора нельзя использовать водный раствор, поскольку вода окисляется при значительно более низком потенциале (+1,32 В) и образующийся фтор стал бы быстро реагировать с водой. Впервые фтор был получен в 1886 г. французским химиком Анри Муассаном при электролизе раствора гидрофторида калия KHF2 в безводной плавиковой кислоте.
В промышленности хлор в основном получают электролизом водного раствора хлорида натрия в специальных электролизёрах. При этом протекают следующие реакции:
полуреакция на аноде: полуреакция на катоде:
Окисление воды на аноде подавляется использованием такого материала электрода, который имеет более высокое перенапряжение по отношению к O2, чем к Cl2 (таким материалом оказался катодное и анодное пространства разделены полимерной ионообменной мембраной. Мембрана позволяет катионам Na+ переходить из анодного пространства в катодное. Переход катионов поддерживает электронейтральность в обеих частях электролизёра, так как в течение электролиза отрицательные ионы удаляются от анода (превращение 2Cl− в Cl2) и накапливаются у катода (образование OH−). Перемещение OH− в противоположную сторону могло бы тоже поддерживать электронейтральность, но ион OH− реагировал бы с Cl2 и сводил на нет весь результат.
Бром получают химическим окислением бромид-иона, находящегося в морской воде. Подобный процесс используется и для получения иода из природных рассолов, богатых I−. В качестве окислителя в обоих случаях используют хлор, обладающий более сильными окислительными свойствами, а образующиеся Br2 и I2 удаляются из раствора потоком воздуха.
Физические свойства галогенов
Фтор является трудносжижаемым, а хлор легкосжижаемым газом с удушливым резким запахом. Энергия связи галогенов сверху вниз по ряду изменяется не равномерно. Фтор имеет аномально низкую энергию связи (151 кДж/моль), это объясняется тем, что фтор не имеет d-подуровня и не способен образовывать полуторные связи, в отличие от остальных галогенов (Cl2 243, Br2 199, I2 150,7, At2117 кДж/моль). От хлора к астату энергия связи постепенно ослабевает, что связано с увеличением атомного радиуса. Аналогичные аномалии имеют и температуры кипения (плавления):
| Простое вещество | Температура плавления, °C | Температура кипения, °C |
| F2 | −220 | −188 |
| Cl2 | −101 | −34 |
| Br2 | −7 | 58 |
| I2 | 113,5 | 184,885 |
| At2 | 244 | 309[2] |
Химические свойства галогенов
Все галогены проявляют высокую окислительную активность, которая уменьшается при переходе от фтора к астату. Фтор — самый активный из галогенов, реагирует со всеми металлами без исключения, многие из них в атмосфере фтора самовоспламеняются, выделяя большое количество теплоты, например:
2Al + 3F2 = 2AlF3 + 2989 кДж, 2Fe + 3F2 = 2FeF3 + 1974 кДж.Без нагревания фтор реагирует и со многими неметаллами (h3, S, С, Si, Р) — все реакции при этом сильно экзотермические, например:
Н2 + F2 = 2HF + 547 кДж, Si + 2F2 = SiF4(г) + 1615 кДж.При нагревании фтор окисляет все другие галогены по схеме
Hal2 + F2 = 2НalFгде Hal = Cl, Br, I, At, причем в соединениях HalF степени окисления хлора, брома, иода и астата равны +1.
Наконец, при облучении фтор реагирует даже с инертными (благородными) газами:
Хе + F2 = XeF2 + 152 кДж.Взаимодействие фтора со сложными веществами также протекает очень энергично. Так, он окисляет воду, при этом реакция носит взрывной характер:
Свободный хлор также очень реакционноспособен, хотя его активность и меньше, чем у фтора. Он непосредственно реагирует со всеми простыми веществами, за исключением кислорода, азота и благородных газов. Для сравнения приведем уравнения реакций хлора с теми же простыми веществами, что и для фтора:
2Al + 3Cl2 = 2AlCl3(кр) + 1405 кДж, 2Fe + ЗCl2 = 2FeCl3(кр) + 804 кДж, Si + 2Cl2 = SiCl4(Ж) + 662 кДж, Н2 + Cl2 = 2HCl(г)+185кДж.Особый интерес представляет реакция с водородом. Так, при комнатной температуре, без освещения хлор практически не реагирует с водородом, тогда как при нагревании или при освещении (например, на прямом солнечном свету) эта реакция протекает со взрывом по приведенному ниже цепному механизму:
Cl2 + hν → 2Cl, Cl + Н2 → HCl + Н, Н + Cl2 → HCl + Cl, Cl + Н2 → HCl + Н и т. д.Возбуждение этой реакции происходит под действием фотонов (hν), которые вызывают диссоциацию молекул Cl2 на атомы — при этом возникает цепь последовательных реакций, в каждой из которых появляется частица, инициирующая начало последующей стадии.
Реакция между Н2 и Cl2 послужила одним из первых объектов исследования цепных фотохимических реакций. Наибольший вклад в развитие представлений о цепных реакциях внёс русский учёный, лауреат Нобелевской премии (1956 год) Н. Н. Семёнов.
Хлор вступает в реакцию со многими сложными веществами, например замещения и присоединения с углеводородами:
СН3-СН3 + Cl2 → СН3-СН2Cl + HCl, СН2=СН2 + Cl2 → СН2Cl — СН2Cl.Хлор способен при нагревании вытеснять бром или иод из их соединений с водородом или металлами:
Cl2 + 2HBr = 2HCl + Br2, Cl2 + 2HI = 2HCl + I2, Cl2 + 2KBr = 2KCl + Br2,а также обратимо реагирует с водой:
Cl2 + Н2О = HCl + HClO — 25 кДж.Хлор, растворяясь в воде и частично реагируя с ней, как это показано выше, образует равновесную смесь веществ, называемую хлорной водой.
Заметим также, что хлор в левой части последнего уравнения имеет степень окисления 0. В результате реакции у одних атомов хлора степень окисления стала −1 (в HCl), у других +1 (в хлорноватистой кислоте HOCl). Такая реакция — пример реакции самоокисления-самовосстановления, или диспропорционирования.
Хлор может таким же образом реагировать (диспропорционировать) со щелочами:
Cl2 + 2NaOH = NaCl + NaClO + Н2О (на холоде), 3Cl2 + 6КОН = 5KCl + KClO3 + 3Н2О (при нагревании).Для примера приведем реакции взаимодействия брома с кремнием и водородом:
Si + 2Br2 = SiBr4(ж) + 433 кДж, Н2 + Br2 = 2HBr(г) + 73 кДж.Являясь более «мягким» реагентом, бром находит широкое применение в органической химии.
Отметим, что бром, так же, как и хлор, растворяется в воде, и, частично реагируя с ней, образует так называемую «бромную воду», тогда как иод практически в воде не растворим и не способен её окислять даже при нагревании; по этой причине не существует «иодной воды». Но иод способен растворяться в растворах иодидов с образованием комплексных анионов:
I2 + I− → I−3.Образующийся раствор называется раствором Люголя.
Иод существенно отличается по химической активности от остальных галогенов. Он не реагирует с большинством неметаллов, а с металлами медленно реагирует только при нагревании. Взаимодействие же иода с водородом происходит только при сильном нагревании, реакция является эндотермической и сильно обратимой:
Н2 + I2 = 2HI — 53 кДж.
Таким образом, химическая активность галогенов последовательно уменьшается от фтора к астату. Каждый галоген в ряду F — At может вытеснять последующий из его соединений с водородом или металлами, то есть каждый галоген в виде простого вещества способен окислять галогенид-ион любого из последующих галогенов. Астат ещё менее реакционноспособен, чем иод. Но и он реагирует с металлами (например с литием):
2Li + At2 = 2LiAt — астатид лития.А при диссоциации образуются не только протоны, но и ионы At+:HAt диссоц. на:2HAt=H++At-+H-+At+.
Примечания
- ↑ Таблица Менделеева на сайте ИЮПАК
- ↑ Редкол.:Кнунянц И. Л. (гл. ред.) Химическая энциклопедия: в 5 т. — Москва: Советская энциклопедия, 1988. — Т. 1. — С. 211. — 623 с. — 100 000 экз.
dic.academic.ru
Галогены - это... Соединения галогенов
Здесь читатель найдет сведения о галогенах, химических элементах периодической таблицы Д. И. Менделеева. Содержание статьи позволит вам ознакомиться с их химическими и физическими свойствами, нахождением в природе, способах применения и др.
Общие сведенья
Галогены – это все элементы химической таблицы Д. И. Менделеева, находящиеся в семнадцатой группе. По более строму способу классификации это все элементы седьмой группы, главной подгруппы.
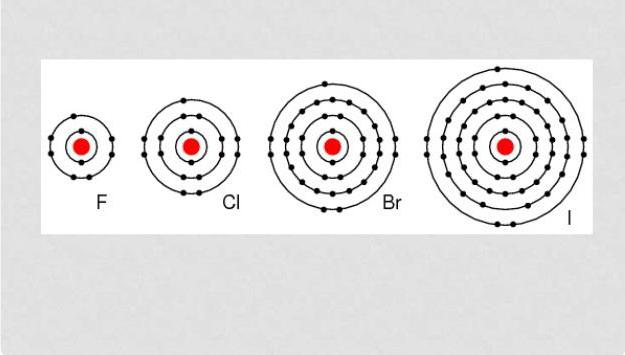
Галогены – это элементы, способные вступать в реакции практически со всеми веществами простого типа за исключением некоторого количества неметаллов. Все они являются энергетическими окислителями, потому в условиях природы, как правило, находятся в смешанной форме с другими веществами. Показатель химической активности галогенов уменьшается с возрастанием их порядковой нумерации.
Галогенами считаются следующие элементы: фтор, хлор, бром, йод, астат и искусственно созданный теннесин.
Как говорилось ранее, все галогены – это окислители с ярко выраженными свойствами, к тому же все они являются неметаллами. Внешний энергетический уровень имеет семь электронов. Взаимодействие с металлами приводит к образованию ионной связи и солей. Почти все галогены, за исключением фтора, могут проявлять себя в качестве восстановителя, достигая высшей окислительной степени +7, однако для этого необходимо, чтобы они взаимодействовали с элементами, имеющими большую степень электроотрицательности.
Особенности этимологии

В 1841 г. шведский ученый-химик Й. Берцелиус предложил ввести термин галогенов, относя к ним известные в то время F, Br, I. Однако до введения этого термина по отношению ко всей группе таких элементов, в 1811 г., немецкий ученый И. Швейггер этим же словом назывался хлор, сам термин переводился с греческого языка как «солерод».
Атомное строение и окислительные степени
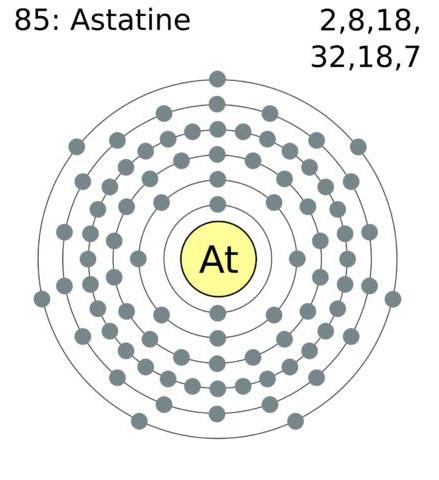
Конфигурация электронов внешней атомной оболочки галогенов имеет следующий вид: астат – 6s26p5, йод – 5s25p5, бром 4s24p5, хлор – 3s23p5, фтор 2s22p5.
Галогены – это элементы, имеющие на электронной оболочке внешнего типа семь электронов, что позволяет им «без особых усилий» присоединять электрон, которого недостаточно для завершения оболочки. Обычно степень окисления проявляется в виде -1. Cl, Br, I и At вступая в реакцию с элементами, имеющими более высокую степень, начинают проявлять положительную окислительную степень: +1, +3, +5, +7. Фтор имеет постоянную окислительную степень -1.
Распространение
Ввиду своей высокой степени реакционной способности галогены обычно находятся в виде соединений. Уровень распространения в коре земли убывает в соответствии с увеличением атомного радиуса от F к I. Астат в коре земли измеряется вовсе в граммах, а теннессин создается искусственно.
Галогены встречаются в природе чаще всего в соединениях галогенидов, а йод также может принимать форму йодата калия или натрия. В связи со своей растворимостью в воде присутствуют в океанических водах и рассолах природного происхождения. F – малорастворимый представитель галогенов и чаще всего обнаруживается в породах осадочного типа, а его главный источник – это фторид кальция.
Физические качественные характеристики
Галогены между собой могут сильно отличаться, и они имеют следующие физические свойства:
- Фтор (F2) – это газ светло-желтого цвета, имеет резкий и раздражающий запах, а также не подвергается сжатию в обычных температурных условиях. Температура плавления равна -220 °С, а кипения -188 °С.
- Хлор (Cl2) представляет собой газ, не сжимающийся при обычной температуре, даже находясь под воздействием давления, имеет удушливый, резкий запах и зелено-желтый окрас. Плавиться начинает при -101 °С, а кипеть при -34 °С.
- Бром (Br2) – это летучая и тяжелая жидкость с буро-коричневым цветом и резким зловонным запахом. Плавится при -7 °С, а кипит при 58 °С.
- Йод (I2) – это вещество твердого типа имеет тёмно-серый окрас, и ему свойственен металлический блеск, запах довольно резкий. Процесс плавления начинается при достижении 113,5 °С, а кипит при 184,885 °С.
- Редкий галоген – это астат (At2), который является твердым веществом и имеет черно-синий цвет с металлическим блеском. Температура плавления соответствует отметке в 244 °С, а кипение начинается после достижения 309 °С.
Химическая природа галогенов
Галогены – это элементы с очень высокой окислительной активностью, которая ослабевает в направлении от F к At. Фтор, будучи самым активным представителем галогенов, реагировать может со всеми видами металлов, не исключая ни один известный. Большинство представителей металлов, попадая в атмосферу фтора, подвергаются самовоспламенению, при этом выделяя теплоту в огромных количествах.
Без подвергания фтора нагреванию он может реагировать с большим количеством неметаллов, например h3, C, P, S, Si. Тип реакций в таком случае является экзотермическим и может сопровождаться взрывом. Нагреваясь, F принуждает окисляться остальные галогены, а подвергаясь облучению, этот элемент способен и вовсе реагировать с тяжелыми газами инертной природы.
Вступая во взаимодействие с веществами сложного типа, фтор вызывает высоко энергетические реакции, например, окисляя воду, он может вызывать взрыв.

Реакционноспособным может быть и хлор, особенно в свободном состоянии. Уровень активности его меньше, чем у фтора, но он способен реагировать почти со всеми простыми веществам, но азот, кислород и благородные газы в реакцию не вступают с ним. Взаимодействуя с водородом, при нагревании или хорошем освещении хлор создает бурнопротекающую реакцию, сопровождаемую взрывом.
В реакциях присоединения и замещения Cl может реагировать с большим количеством веществ сложного типа. Способен вытеснять Br и I в результате нагревания из соединений, созданных ими с металлом или водородом, а также может вступать в реакцию со щелочными веществами.
Бром химически менее активный, чем хлор или фтор, но все же весьма ярко себя проявляет. Это обусловлено тем, что чаще всего бром Br используется в качестве жидкости, ведь в таком состоянии исходная степень концентрации при остальных одинаковых условиях выше, чем у Cl. Широко используется в химии, особенно органической. Может растворяться в h3O и реагировать с ней частично.
Галоген-элемент иод образует простое вещество I2 и способен вступать в реакции с h3O, растворяется в йодидах растворов, образуя при этом комплексные анионы. От большинства галогенов I отличается тем, что он не вступает в реакции с большинством представителей неметаллов и не спеша реагирует с металлами, при этом его необходимо нагревать. С водородом реагирует, лишь подвергаясь сильному нагреванию, а реакция является эндотермической.
Редкий галоген астат (At) проявляет реакционные способности меньше йода, однако может реагировать с металлами. В результате диссоциации возникают как анионы, так и катионы.
Области применения
Соединения галогенов широко применяются человеком в самых разнообразных областях деятельности. Природный криолит (Na3AlF6) используют для получения Al. Бром и йод в качестве простых веществ часто используют фармацевтические и химические компании. При производстве запчастей для машин часто используют галогены. Фары – это одна из таких деталей. Качественно выбрать материал для данной составной части машины очень важно, так как фары освещают дорогу в ночное время и являются способом обнаружения как вас, так и других автомобилистов. Одним из лучших составных материалов для создания фар считается ксенон. Галоген тем не менее ненамного уступает по качеству этому инертному газу.

Хороший галоген – это фтор, добавка, широко используемая при производстве зубных паст. Он помогает предотвращать возникновение заболевания зубов – кариеса.
Такой элемент-галоген, как хлор (Cl), находит свое применение в получении HCl, часто используется при синтезе органических веществ, таких как пластмасса, каучук, синтетические волокна, красители и растворители и т. д. А также соединения хлора используют в качестве отбеливателей льняного и хлопчатобумажного материала, бумаги и как средство для борьбы с бактериями в питьевой воде.

Внимание! Токсично!
Ввиду наличия очень высокой реакционной способности галогены по праву называются ядовитыми. Наиболее ярко способность к вступлению в реакции выражена у фтора. Галогены имеют ярко выраженные удушающие свойства и способны поражать ткани при взаимодействии.
Фтор в парах и аэрозолях считается одним из самых потенциально опасных форм галогенов, вредоносных для окружающих живых существ. Это связано с тем, что он слабо воспринимается обонянием и ощущается лишь по достижении большой концентрации.
Подводя итоги
Как мы видим, галогены являются очень важной частью периодической таблицы Менделеева, они имеют множество свойств, отличаются между собой по физическим и химическим качествам, атомному строению, степени окисления и способности реагировать с металлами и неметаллами. В промышленности используются разнообразным образом, начиная от добавок в средства личной гигиены и заканчивая синтезом веществ органической химии или отбеливателями. Несмотря на то что одним из лучших способов поддержания и создания света в фаре автомобиля является ксенон, галоген тем не менее ему практически не уступает и также широко используется и имеет свои преимущества.
Теперь вы знаете, что такое галоген. Сканворд с любыми вопросами об этих веществах для вас уже не помеха.
fb.ru
Что такое галогены? Химические элементы фтор, хлор, иод и астат
Все элементы периодической таблицы Менделеева объединяют в группы, в зависимости от их химических свойств. В данной статье мы разберем, что такое галогены (или галоиды).
Значение понятия галогены
Галогены – это элементы из периодической таблицы Менделеева 17 группы, а по устаревшей классификации – 7 главной подгруппы. К галогенам относится всего 5 химических элементов, среди которых фтор, хлор, иод, астат и бром. Все они являются неметаллами. Галогены – очень активные окислители, а на внешнем уровне данные элементы имеют по 7 электронов.
Что такое галогены, почему они получили такое название? Слово «галоген» образовалось от двух греческих слов, которые в совокупности означают «рождение соли». Один из элементов этой группы – хлор, вместе с натрием образует соль.
Физические свойства группы галогенов
Химические свойства галогенов схожи, но по физическим характеристикам элементы отличаются друг от друга.
Фтор – это газообразное вещество желтого цвета, с очень неприятным и резким запахом. Хлор – газ зелено-желтого цвета, имеет тяжелый и отталкивающий аромат. Бром – жидкость коричневого цвета. Астат – иссиня-чёрное твердое вещество с резким запахом. Йод – серое твердое вещество. Резюмируя вышеозначенную информацию, можно ответить на вопрос: «Что такое галогены?». Это и газы, и жидкости, и твердые тела.

Химические свойства группы галогенов
Основным общим свойством всех галогенов является то, что они все очень активные окислители. Самым активным галоидом является фтор, который реагирует со всеми металлами, а самый неактивный – астат.
Взаимодействие с галогенами у простых веществ (исключение составляют некоторые неметаллы) проходит легко. В природе они встречаются только в виде соединений.
Фтор
Такой химический элемент, как фтор был получен лишь в конце XIX века французским ученым по имени Анри Муассан. Фтор – это газ бледно-желтого цвета. Галогены являются типичными неметаллами и окислителями, а фтор из всех галогенов - самый активный. Сейчас этот галоген незаменим в промышленности ведь его используют при изготовлении труб, изоленты, различных тканевых покрытий, антипригарных поверхностей для сковородок и форм, а в медицине при изготовлении искусственных артерий и вен. В промышленности этот галоген разбавляют азотом.

Хлор
Хлор – знаменитый химический элемент, относится к группе галогенов. Что такое галогены, мы разобрали выше. Хлор сохраняет основные свойства элементов своей группы.
Название он получил от греческого слова «хлорос», что переводится как бледно-зеленый. Этот газ очень широко распространен в природе, он в больших количествах содержится в морской воде. Хлор – очень важный химический элемент, он практически незаменим при отбеливании, дезинфекции бассейнов, а также обеззараживанию питьевой воды.
Но хлор также известен и тем, что является опаснейшим смертельным оружием. В 1915 году немецкие войска использовали против французской армии порядка 6 тыс. баллонов с этим галогеном. Это смертельное оружие было придумано известным немецким химиком Фрицом Хабером.

Йод
Йод, или иод, – еще один химический элемент, который относится к группе галогенов. На самом деле в таблице Менделеева этот элемент называется не иначе как иод, но его тривиальным названием принято считать йод. Наименование элемента произошло от греческого слова, что в переводе на русский означает «фиалковый». Этот химический элемент в повседневной жизни встречается довольно часто. При взаимодействии с другими галогенами в основном с хлором получается отличное средство для дезинфекции ран и царапин. Сейчас иод применяют в медицине для профилактики болезней щитовидной железы.
Астат
Астат интересен тем, что никогда не был получен химиками в таком количестве, чтобы его можно было увидеть невооруженным глазом. И скорее всего, эта возможность никогда им не представится. Если бы специалисты и смогли получить большое количество этого химического элемента, он тут же и испарился бы, по причине возникновения высокой температуры, которая появляется в результате радиоактивного излучения этого элемента. Астат – самый редкий химический элемент, а небольшое его количество содержится в земной коре.
Среди галогенов астат – довольно бесполезный элемент, потому что на данный момент никакого применения ему не найдено.
Применение и значение
Несмотря на то что все галогены имеют схожие химические свойства, применяются они совершенно в разных сферах. Например, фтор очень полезен для зубов, именно поэтому его добавляют в зубные пасты. Применение лечебных и профилактических средств, в составе которых присутствует химический элемент фтор, предотвращает появление кариеса. Хлор используют для получения соляной кислоты, которая незаменима в промышленности и медицине. Хлор используют для изготовления каучука, пластмассы, растворителей, красителей, а также синтетических волокон. Соединения, в которых содержится этот элемент, используют в сельском хозяйстве для борьбы с вредителями. Галоген хлор незаменим для отбеливания бумаги и тканей. Считается, что применение хлора для обработки питьевой воды небезопасно. Бром, который является галогеном, а также иод часто используют в медицине.

Значение галогенов в жизни человека огромно. Если представить существование человечества без галоидов, то мы были бы лишены таких вещей, как фотографии, антисептические и дезинфицирующие средства, каучук, пластик, линолеум и многих других. Помимо этого, данные вещества необходимы организму человека, чтобы нормально функционировать, то есть играют важную биологическую роль. Хоть свойства галогенов и схожи, их роль в промышленности и медицине разная.
fb.ru
Слово ГАЛОГЕН - Что такое ГАЛОГЕН?
Слово галоген английскими буквами(транслитом) - galogen
Слово галоген состоит из 7 букв: а г г е л н о
Значения слова галоген. Что такое галоген?
Галогены
ГАЛОГЕНЫ ПОДГРУППА VIIA. ГАЛОГЕНЫ ФТОР, ХЛОР, БРОМ, ИОД, АСТАТ Галогены и особенно фтор, хлор и бром имеют большое значение для промышленности и лабораторной практики как в свободном состоянии…
Энциклопедия КольераГАЛОГЕНЫ (от греч. hals, род. падеж halos - соль и -genes-рождающий, рождённый) (галоиды), хим. элементы главной подгруппы VII гр. периодич. системы: фтор, хлор, бром, иод и астат.
Химическая энциклопедияГАЛОГЕНЫ, элементы (ФТОР, ХЛОР, БРОМ, ЙОД и АСТАТ), принадлежащие к VII группе периодической таблицы. Они реагируют с большинством других элементов и органическими соединениями.
Научно-технический энциклопедический словарьГалогениды
ГАЛОГЕНИДЫ, хим. соед. галогенов с др. элементами. К галогенидам обычно относят соед., в к-рых атомы галогена имеют большую электроотрицательность, чем др. элемент.
Химическая энциклопедияГАЛОГЕНИДЫ , хим. соед. галогенов с др. элементами. К Г. обычно относят соед., в к-рых атомы галогена имеют большую электроотрицательность, чем др. элемент.
Химическая энциклопедия. - 1988Галогени́ды (галоиды) — соединения галогенов с другими химическими элементами или радикалами. При этом галоген, входящий в соединение, должен быть электроотрицательным; так, оксид брома не является галогенидом.
ru.wikipedia.orgГалогенирование
ГАЛОГЕНИРОВАНИЕ (галоидирование), введение галогена в молекулу орг. соединения. Осуществляют путем р-ций замещения (заместительное Г.) или присоединения (присоединительное Г.).
Химическая энциклопедия. - 1988ГАЛОГЕНИРОВАНИЕ (галоидирование), введение галогена в молекулу орг. соединения. Осуществляют путем р-ций замещения (заместительное галогенирование) или присоединения (присоединительное галогенирование)..
Химическая энциклопедияГАЛОГЕНИРОВАНИЕ, введение ГАЛОГЕНОВ (фтора, хлора, брома, йода или астата) в органическое соединение путем присоединения или замещения атома или группы атомов.
Научно-технический энциклопедический словарьДегалогенирование
ДЕГАЛОГЕНИРОВАНИЕ — элиминирование галогена из молекулы орг. соед. или замещение его на атом Н. Элиминирование атомов галогена может протекать с отщеплением галогена от соседних атомов С в соед. алифатич.
Химическая энциклопедия. - 1988ДЕГАЛОГЕНИРОВАНИЕ, элиминирование галогена из молекулы орг. соед. или замещение его на атом Н. Элиминирование атомов галогена может протекать с отщеплением галогена от соседних атомов С в соед. алифатич.
Химическая энциклопедияГАЛОГЕНЗАМЕЩЕННЫЕ УГЛЕВОДОРОДОВ
ГАЛОГЕНЗАМЕЩЕННЫЕ УГЛЕВОДОРОДОВ, орг. соед., в молекулах к-рых содержатся атомы галогенов, связанные с углеводородными радикалами (алифатич., ароматич. и алициклическими).
Химическая энциклопедияГАЛОГЕНЗАМЕЩЕННЫЕ УГЛЕВОДОРОДОВ — орг. соед., в молекулах к-рых содержатся атомы галогенов, связанные с углеводородными радикалами (алифатич., ароматич. и алициклическими).
Химическая энциклопедия. - 1988Галоиды или галогены
Галоиды или галогены (хим.). — Так называются четыре элементарных тела, находящихся в седьмой группе периодической системы элементов: фтор F = 19, хлор Сl = 3,5, бром Br = 80 и йод J = 127.
Энциклопедический словарь Ф.А. Брокгауза и И.А. Ефрона. - 1890-1907Русский язык
Гал/о/ге́н/.
Морфемно-орфографический словарь. — 2002- галогенный
- галогеноводород
- галогенопроизводный
- галоген
- галоидирование
- галоидный
- галоид
wordhelp.ru
физические свойства, химические свойства. Применение галогенов и их соединений
Галогены в периодической таблице расположены слева от благородных газов. Эти пять токсических неметаллических элементов входят в 7 группу периодической таблицы. К ним относятся фтор, хлор, бром, йод и астат. Хотя астат радиоактивен и имеет только короткоживущие изотопы, он ведет себя, как йод, и его часто причисляют к галогенам. Поскольку галогенные элементы имеют семь валентных электронов, им необходим лишь один дополнительный электрон для образования полного октета. Эта характеристика делает их более активными, чем другие группы неметаллов.
Общая характеристика
Галогены образуют двухатомные молекулы (вида Х2, где Х обозначает атом галогена) – устойчивую форму существования галогенов в виде свободных элементов. Связи этих двухатомных молекул являются неполярными, ковалентными и одинарными. Химические свойства галогенов позволяют им легко вступать в соединение с большинством элементов, поэтому они никогда не встречаются в несвязанном виде в природе. Фтор – наиболее активный галоген, а астат – наименее.
Все галогены образуют соли I группы с похожими свойствами. В этих соединениях галогены присутствуют в виде галоидных анионов с зарядом -1 (например, Cl-, Br-). Окончание -ид указывает на наличие галогенид-анионов; например Cl- называется «хлорид».
Кроме того, химические свойства галогенов позволяют им действовать в качестве окислителей – окислять металлы. Большинство химических реакций, в которых участвуют галогены – окислительно-восстановительные в водном растворе. Галогены образуют одинарные связи с углеродом или азотом в органических соединениях, где степень их окисления (СО) равна -1. Когда атом галогена замещён ковалентно-связанным атомом водорода в органическом соединении, префикс гало- может быть использован в общем смысле, или префиксы фтор-, хлор-, бром- , йод- – для конкретных галогенов. Галогенные элементы могут иметь перекрёстную связь с образованием двухатомных молекул с полярными ковалентными одинарными связями.
Хлор (Cl2) стал первым галогеном, открытым в 1774 г., затем были открыты йод (I2), бром (Br2), фтор (F2) и астат (At, обнаружен последним, в 1940 г.). Название «галоген» происходит от греческих корней hal- («соль») и -gen («образовывать»). Вместе эти слова означают «солеобразующий», подчёркивая тот факт, что галогены, вступая в реакцию с металлами, образуют соли. Галит – это название каменной соли, природного минерала, состоящего из хлорида натрия (NaCl). И, наконец, галогены используются в быту – фторид содержится в зубной пасте, хлор обеззараживает питьевую воду, а йод содействует выработке гормонов щитовидной железы.
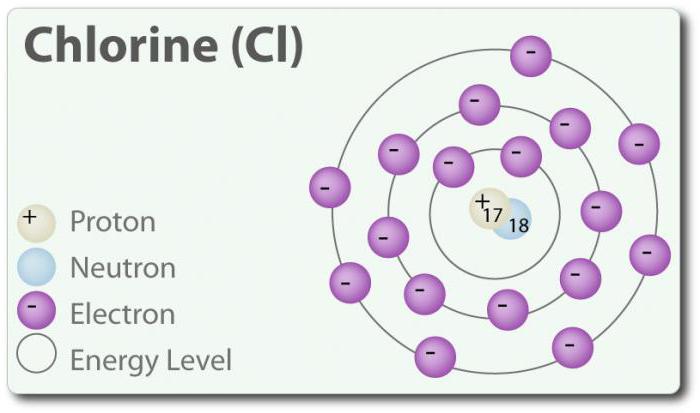
Химические элементы
Фтор – элемент с атомным номером 9, обозначается символом F. Элементарный фтор впервые был обнаружен в 1886 г. путем выделения его из плавиковой кислоты. В свободном состоянии фтор существует в виде двухатомной молекулы (F2) и является наиболее распространенным галогеном в земной коре. Фтор – наиболее электроотрицательный элемент в периодической таблице. При комнатной температуре является бледно-жёлтым газом. Фтор также имеет относительно небольшой атомный радиус. Его СО – -1, за исключением элементарного двухатомного состояния, в котором его степень окисления равна нулю. Фтор чрезвычайно химически активен и непосредственно взаимодействует со всеми элементами, кроме гелия (He), неона (Ne) и аргона (Ar). В растворе h3O, плавиковой кислоты (HF) является слабой кислотой. Хотя фтор сильно электроотрицателен, его электроотрицательность не определяет кислотность; HF является слабой кислотой в связи с тем, что ион фтора основной (рН> 7). Кроме того, фтор производит очень мощные окислители. Например, фтор может вступать в реакцию с инертным газом ксеноном и образует сильный окислитель дифторид ксенона (XeF2). У фтора множество применений.
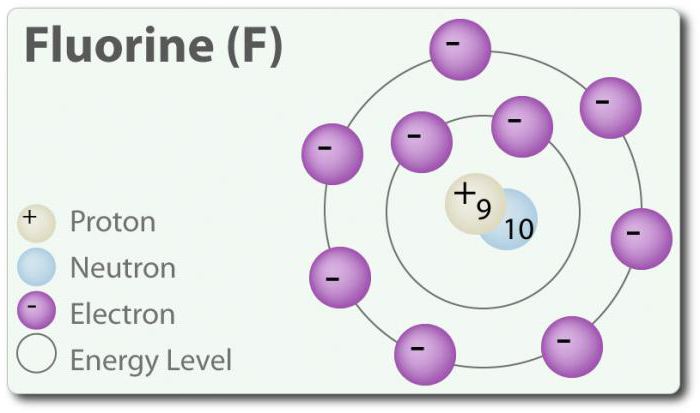
Хлор – элемент с атомным номером 17 и химическим символом Cl. Обнаружен в 1774 г. путём выделения его из соляной кислоты. В своём элементарном состоянии он образует двухатомную молекулу Cl2. Хлор имеет несколько СО: -1, +1, 3, 5 и 7. При комнатной температуре он является светло-зеленым газом. Так как связь, которая образуется между двумя атомами хлора, является слабой, молекула Cl2 обладает очень высокой способностью вступать в соединения. Хлор реагирует с металлами с образованием солей, которые называются хлориды. Ионы хлора являются наиболее распространенными ионами, они содержатся в морской воде. Хлор также имеет два изотопа: 35Cl и 37Cl. Хлорид натрия является наиболее распространенным соединением из всех хлоридов.
Бром – химический элемент с атомным номером 35 и символом Br. Впервые был обнаружен в 1826 г. В элементарной форме бром является двухатомной молекулой Br2. При комнатной температуре представляет собой красновато-коричневую жидкость. Его СО – -1, + 1, 3, 4 и 5. Бром более активен, чем йод, но менее активен, чем хлор. Кроме того, бром имеет два изотопа: 79Вг и 81Вг. Бром встречается в виде солей бромида, растворённых в морской воде. За последние годы производство бромида в мире значительно увеличилось благодаря его доступности и продолжительному времени жизни. Как и другие галогены, бром является окислителем и очень токсичен.
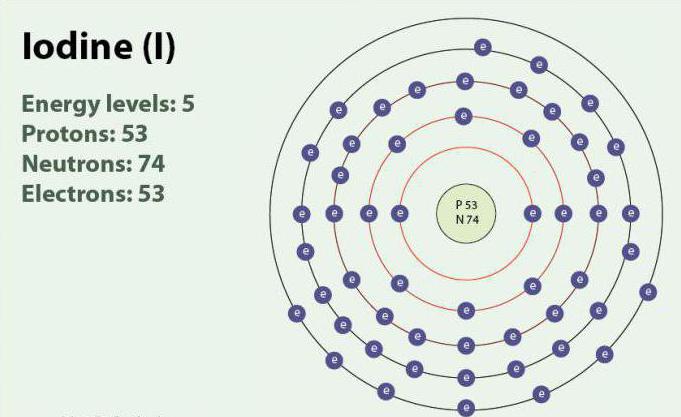
Йод – химический элемент с атомным номером 53 и символом I. Йод имеет степени окисления: -1, +1, +5 и +7. Существует в виде двухатомной молекулы, I2. При комнатной температуре является твёрдым веществом фиолетового цвета. Йод имеет один стабильный изотоп - 127I. Впервые обнаружен в 1811 г. с помощью морских водорослей и серной кислоты. В настоящее время ионы йода, могут быть выделены в морской воде. Несмотря на то что йод не очень хорошо растворим в воде, его растворимость может возрасти при использовании отдельных йодидов. Йод играет важную роль в организме, участвуя в выработке гормонов щитовидной железы.
Астат – радиоактивный элемент с атомным номером 85 и символом At. Его возможные степени окисления: -1, +1, 3, 5 и 7. Единственный галоген, не являющийся двухатомной молекулой. В нормальных условиях является металлическим твёрдым веществом чёрного цвета. Астат является очень редким элементом, поэтому о нём известно немного. Кроме того, астат имеет очень короткий период полураспада, не дольше нескольких часов. Получен в 1940 г. в результате синтеза. Полагают, что астат похож на йод. Отличается металлическими свойствами.
В таблице ниже показано строение атомов галогенов, структура внешнего слоя электронов.
Галоген | Конфигурация электронов |
Фтор | 1s2 2s2 2p5 |
Хлор | 3s2 3p5 |
Бром | 3d10 4s2 4p5 |
Иод | 4d10 5s2 5p5 |
Астат | 4f14 5d10 6s2 6p5 |
Подобное строение внешнего слоя электронов обусловливает то, что физические и химические свойства галогенов похожи. Вместе с тем при сопоставлении этих элементов наблюдаются и различия.
Периодические свойства в группе галогенов
Физические свойства простых веществ галогенов изменяются с повышением порядкового номера элемента. Для лучшего усвоения и большей наглядности мы предлагаем вам несколько таблиц.
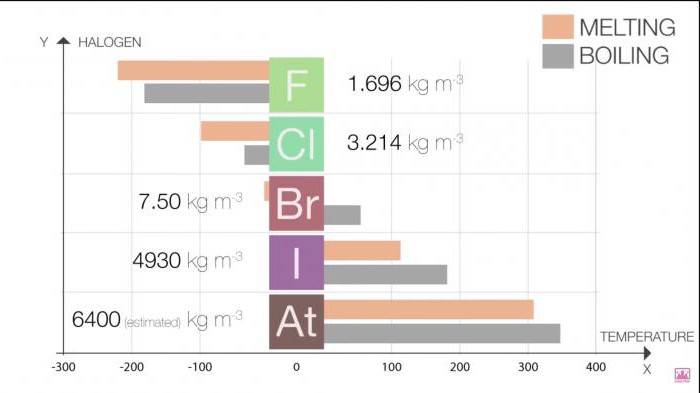
Точки плавления и кипения в группе возрастают по мере роста размера молекулы (F <Cl <Br <I <At). Это увеличение означает увеличение силы Ван-дер-Ваальса.
Таблица 1. Галогены. Физические свойства: точки плавления и кипения
Галоген | Т плавления (˚C) | Т кипения (˚C) |
Фтор | -220 | -188 |
Хлор | -101 | -35 |
Бром | -7.2 | 58.8 |
Иод | 114 | 184 |
Астат | 302 | 337 |
- Атомный радиус увеличивается.
Размер ядра увеличивается (F < Cl < Br < I < At), так как увеличивается число протонов и нейтронов. Кроме того, с каждым периодом добавляется всё больше уровней энергии. Это приводит к большей орбитали, и, следовательно, к увеличению радиуса атома.
Таблица 2. Галогены. Физические свойства: атомные радиусы
Галоген | Ковалентный радиус (пм) | Ионный (X-) радиус (пм) |
Фтор | 71 | 133 |
Хлор | 99 | 181 |
Бром | 114 | 196 |
Иод | 133 | 220 |
Астат | 150 |
- Энергия ионизации уменьшается.
Если внешние валентные электроны не находятся вблизи ядра, то для их удаления от него не потребуется много энергии. Таким образом, энергия, необходимая для выталкивания внешнего электрона не столь высока в нижней части группы элементов, так как здесь больше энергетических уровней. Кроме того, высокая энергия ионизации заставляет элемент проявлять неметаллические качества. Йод и дисплей астат проявляют металлические свойства, потому что энергия ионизации снижается (At < I < Br < Cl < F).
Таблица 3. Галогены. Физические свойства: энергия ионизации
Галоген | Энергия ионизации (кДж/моль) |
фтор | 1681 |
хлор | 1251 |
бром | 1140 |
йод | 1008 |
астат | 890±40 |
- Электроотрицательность уменьшается.
Число валентных электронов в атоме возрастает с увеличением уровней энергии при прогрессивно более низких уровнях. Электроны прогрессивно дальше от ядра; Таким образом, ядро и электроны не как притягиваются друг к другу. Увеличение экранирования наблюдается. Поэтому Электроотрицательность уменьшается с ростом периода (At < I < Br < Cl < F).
Таблица 4. Галогены. Физические свойства: электроотрицательность
Галоген | Электроотрицательность |
фтор | 4.0 |
хлор | 3.0 |
бром | 2.8 |
иод | 2.5 |
астат | 2.2 |
- Сродство к электрону уменьшается.
Так как размер атома увеличивается с увеличением периода, сродство к электрону, как правило, уменьшается (В < I < Br < F < Cl). Исключение – фтор, сродство которого меньше, чем у хлора. Это можно объяснить меньшим размером фтора по сравнению с хлором.
Таблица 5. Сродство галогенов к электрону
Галоген | Сродство к электрону (кДж/моль) |
фтор | -328.0 |
хлор | -349.0 |
бром | -324.6 |
иод | -295.2 |
астат | -270.1 |
- Реактивность элементов уменьшается.
Реакционная способность галогенов падает с ростом периода (At <I <Br <Cl <F). Это связано с увеличением радиуса атома с возрастанием уровней энергии электронов. Это снижает притяжение валентных электронов других атомов, снижая реакционную способность. Это уменьшение также происходит из-за падения электроотрицательности с увеличением периода, что также снижает притяжение электронов. Кроме того, с увеличением размера атома снижается и окислительная способность.
Неорганическая химия. Водород + галогены
Галогенид образуется, когда галоген реагирует с другим, менее электроотрицательным элементом с образованием бинарного соединения. Водород реагирует с галогенами, образуя галогениды вида НХ:
- фтороводород HF;
- хлороводород HCl;
- бромоводород HBr;
- иодоводород HI.
Галогениды водорода легко растворяются в воде с образованием галогенводородной (плавиковой, соляной, бромистоводородной, иодистоводородной) кислоты. Свойства этих кислот приведены ниже.
Кислоты образуются следующей реакцией: HX (aq) + h3O (l) → Х- (aq) + h4O+ (aq).
Все галоидоводороды образуют сильные кислоты, за исключением HF.
Кислотность галогеноводородных кислот увеличивается: HF <HCl <HBr <HI.
Плавиковая кислота способна гравировать стекло и некоторые неорганические фториды длительное время.
Может показаться нелогичным, что HF является самой слабой галогенводородной кислотой, так как фтор обладает самой высокой электроотрицательностью. Тем не менее связь Н-F очень сильна, в результате чего кислота очень слабая. Сильная связь определяется короткой длиной связи и большой энергией диссоциации. Из всех галогенидов водорода HF имеет самую короткую длину связи и самую большую энергию диссоциации связи.
Галогенные оксокислоты
Галогенные оксокислоты представляют собой кислоты с атомами водорода, кислорода и галогена. Их кислотность может быть определена с помощью анализа структуры. Галогенные оксокислоты приведены ниже:
- Хлорноватистая кислота HOCl.
- Хлористая кислота HClO2.
- Хлорноватая кислота HClO3.
- Хлорная кислота HClO4.
- Бромноватистая кислота HOBr.
- Бромноватая кислота HBrO3.
- Бромная кислота HBrO4.
- Иодноватистая кислота HOI.
- Йодноватая кислота HIO3.
- Метайодная кислота HIO4, H5IO6.
В каждой из этих кислот протон связан с атомом кислорода, поэтому сравнение длин связей протонов здесь бесполезно. Доминирующую роль здесь играет электроотрицательность. Активность кислотны возрастает с увеличением числа атомов кислорода, связанный с центральным атомом.
Внешний вид и состояние вещества
Основные физические свойства галогенов кратко можно выразить в следующей таблице.
Состояние вещества (при комнатной температуре) | Галоген | Внешний вид |
твёрдое | йод | фиолетовый |
астат | чёрный | |
жидкое | бром | красно-коричневый |
газообразное | фтор | бледно-жёлто-коричневый |
хлор | бледно-зелёный |
Объяснение внешнего вида
Цвет галогенов является результатом поглощения видимого света молекулами, что вызывает возбуждение электронов. Фтор поглощает фиолетовый свет, и, следовательно, выглядит светло-жёлтым. Йод, наоборот, поглощает жёлтый свет и выглядит фиолетовым (жёлтый и фиолетовый – дополняющие цвета). Цвет галогенов становится темнее с ростом периода.
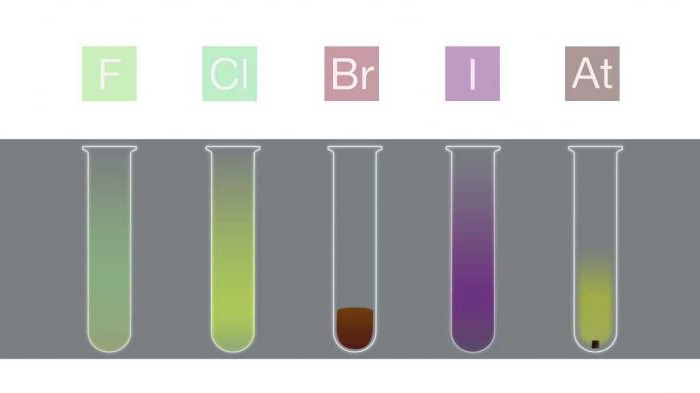
В закрытых ёмкостях жидкий бром и твёрдый йод находятся в равновесии со своими парами, которые можно наблюдать в виде цветного газа.
Хотя цвет астата неизвестен, предполагается, что он должен быть темнее йода (т. е. черным) в соответствии с наблюдаемой закономерностью.
Теперь, если вас попросят: «Охарактеризуйте физические свойства галогенов», вам будет что сказать.
Степень окисления галогенов в соединениях
Степень окисления часто используется вместо понятия "валентность галогенов". Как правило, степень окисления равна -1. Но если галоген связан с кислородом или другим галогеном, он может принимать другие состояния: СО кислорода -2 имеет приоритет. В случае двух различных атомов галогена, соединенных вместе, более электроотрицательный атом превалирует и принимает СО -1.
Например, в хлориде йода (ICl) хлор имеет СО -1, и йод +1. Хлор является более электроотрицательным, чем йод, поэтому его СО равна -1.
В бромной кислоте (HBrO4) кислород обладает СО -8 (-2 х 4 атома = -8). Водород имеет общую степень окисления +1. Сложение этих значений даёт СО -7. Так как конечное СО соединения должно быть нулевым, то СО брома равна +7.
Третьим исключением из правила является степень окисления галогена в элементарной форме (X2), где его СО равна нулю.
Галоген | СО в соединениях |
фтор | -1 |
хлор | -1, +1, +3, +5, +7 |
бром | -1, +1, +3, +4, +5 |
йод | -1, +1, +5, +7 |
астат | -1, +1, +3, +5, +7 |
Почему СО фтора всегда -1?
Электроотрицательность увеличивается с ростом периода. Поэтому фтор имеет самую высокую электроотрицательность из всех элементов, что подтверждается его положением в периодической таблице. Его электронная конфигурация 1s2 2s2 2p5. Если фтор получает еще один электрон, крайние р-орбитали полностью заполнены и составляют полный октет. Поскольку фтор имеет высокую электроотрицательность, он может легко отобрать электрон у соседнего атома. Фтор в этом случае изоэлектронен инертному газу (с восемью валентными электронами), все его внешние орбитали заполнены. В таком состоянии фтор гораздо более стабилен.
Получение и применение галогенов
В природе галогены находятся в состоянии анионов, поэтому свободные галогены получают методом окисления путём электролиза или с помощью окислителей. Например, хлор вырабатывается гидролизом раствора поваренной соли. Применение галогенов и их соединений многообразно.
- Фтор. Несмотря на то что фтор очень реактивен, он используется во многих областях промышленности. Например, он является ключевым компонентов политетрафторэтилена (тефлона) и некоторых других фторполимеров. Хлорфторуглероды представляют собой органические химические вещества, которые ранее использовались в качестве хладагентов и пропеллентов в аэрозолях. Их применение прекратилось из-за возможного их воздействия на окружающую среду. Их заменили гидрохлорфторуглероды. Фтор добавляют в зубную пасту (SnF2) и питьевую воду (NaF) для предотвращения разрушения зубов. Этот галоген содержится в глине, используемой для производства некоторых видов керамики (LiF), используется в ядерной энергетике (UF6), для получения антибиотика фторхинолона, алюминия (Na3AlF6), для изоляции высоковольтного оборудования (SF6).
- Хлор также нашёл разнообразное применение. Он используется для дезинфекции питьевой воды и плавательных бассейнов. Гипохлорит натрия (NaClO) является основным компонентом отбеливателей. Соляная кислота широко используется в промышленности и лабораториях. Хлор присутствует в поливинилхлориде (ПВХ) и других полимерах, которые используются для изоляции проводки, труб и электроники. Кроме того, хлор оказался полезен и в фармацевтической промышленности. Лекарственные средства, содержащие хлор, используются для лечения инфекций, аллергии и диабета. Нейтральная форма гидрохлорида – компонент многих препаратов. Хлор используется также для стерилизации больничного оборудования и дезинфекции. В сельском хозяйстве хлор является компонентом многих коммерческих пестицидов: ДДТ (дихлородифенилтрихлорэтан) использовался в качестве сельскохозяйственного инсектицида, но его использование было прекращено.

- Бром, благодаря своей негорючести, применяется для подавления горения. Он также содержится в бромистом метиле, пестициде, используемом для хранения урожая и подавления бактерий. Однако чрезмерное использование бромистого метила было прекращено из-за его воздействия на озоновый слой. Бром применяют при производстве бензина, фотоплёнки, огнетушителей, лекарств для лечения пневмонии и болезни Альцгеймера.
- Йод играет важную роль в надлежащем функционировании щитовидной железы. Если организм не получает достаточного количества йода, происходит увеличение щитовидной железы. Для профилактики зоба данный галоген добавляют в поваренную соль. Йод также используется в качестве антисептического средства. Йод содержится в растворах, используемых для очистки открытых ран, а также в дезинфицирующих спреях. Кроме того, йодид серебра имеет важное значение в фотографии.
- Астат – радиоактивный и редкоземельный галоген, поэтому ещё нигде не используется. Тем не менее полагают, что этот элемент может помочь йоду в регуляции гормонов щитовидной железы.
fb.ru
Галогены и галогенный газ: химические особенности галогенов
Галогены – так обозначаются элементы химической таблицы Менделеева, расположенные в семнадцатой группе. Особенность в том, что они вступают в реакцию почти что со всеми веществами простого типа, исключая лишь определенные неметаллы. Так как они выступают в роли энергетических окислителей, в природе они смешиваются с другими веществами. Химическая активность галогенов напрямую зависит от порядкового номера.
Что такое галогены
Общие сведения о галогенах
Галогенами называют данные элементы: фтор, хлор, бром, йод и астат. Все они относятся к ярко выраженным неметаллам. Только лишь в йоде можно при определенных обстоятельствах обнаружить свойства, приписываемые металлам.
Изначально был использован термин «галоген» в 1811 году немецким ученым И. Швейггером, который дословно с греческого переводится как «солерод».
Будучи в основном состоянии электронная конфигурация атомов галогенов следующая – ns 2 np 5, где буквой n отмечается главное квантовое число или период. Если сравнить атом хлора с остальными галогенами, будет заметно, что его электроны слабо экранированы от ядра, из-за чего тот характеризуется высокой удельной электронной плотностью и меньшим радиусом, а также имеет большие значения энергии ионизации и электроотрицательности.
Фтор (F) – элемент, доступный в виде солей, которые рассеяны по разным горным породам. Наиболее важное соединение – минерал флюорит и плавиковый шпат. Также небезызвестен минерал криолит.
Хлор (Cl) – является наиболее распространенным галогеном. Его важнейшим природным соединением считается хлорид натрия, который применяется в качестве основного сырья, если нужно получить другие хлористые соединения. Хлорид натрия в большей массе распространен в водах морей и океанов, но встретить его можно и в некоторых озерах. Отыскать данный галоген можно и в твердом виде, так называемой каменной соли.
Бром (Br) – в условиях природы имеет вид солей натрия и калия в паре с хлористыми солями. Как правило, встречается в соленых озерах и морях.
Йод (J) – химический элемент, который также нередко встречается в морской воде, но в очень малых количествах, поэтому выделение его из влаги – процедура достаточно затруднительная. Заметим, что существует определенный вид морских водорослей – ламинарии, в их тканях происходит накопление йода. Из золы этих водорослей и добывается йод. Встретить йод можно и в буровых водах, пролегающих под землей.
Астат (At) – практически не встречаемый в условиях природы химический элемент. Чтобы его добыть, искусственно осуществляются ядерные реакции. У астата имеется самый долгоживущий изотоп, период полураспада которого составляет 8.3 часа.
Химические особенности галогенов
Внешний вид галогенов
Задавая вопрос, галогены – что это такое, следует ответить, что это все элементы Менделеевской таблицы, где у каждого есть свой собственный показатель химической активности. При рассмотрении последней у фтора следует отметить, что она максимально высокая. Академик А.Е. Ферсман называет фтор всесъедающим. Так, если взять комнатную температуру, то в атмосфере фтора будут сгорать железо, свинец и щелочные металлы.
Важно! Фтор не оказывает никакого воздействия на определенные металлы (медь, никель), на поверхности которых образуется защитный слой в виде фторида. Но если нагреть фтор, реакция начнет появляться.
Отметим реакцию фтора на многие неметаллы, среди которых водород, йод, углерод, бор и другие. В условиях холода образуются соответствующие соединения, которые способны привести к взрыву или образованию пламени. Фтор не способен реагировать лишь на кислород, азот и углерод (последний должен быть в виде алмаза).
Очень энергичная реакция замечена на сложные вещества. В атмосфере фтора сгорают даже довольно стойкие вещества в виде стекла (вата) и водяного пара. Следует заметить, что фтор нельзя растворить в воде, так как он способен ее энергично растворять.
Обратите внимание! Фтор является самым сильным окислителем.
Каждые галогенные соединения имеют свои особенности, так, у хлора также заметна высокая химическая активность, хоть и уступающая фтору. Данный элемент способен оказывать действие на все простые вещества, исключая лишь кислород, азот и благородные газы. В условиях высокой температуры следующие неметаллы: фосфор, мышьяк, кремний и сурьма, вступая в реакцию с хлором, выделяют большое количество тепла. В условиях комнатной температуры и без света хлор почти что не оказывает воздействия на водород, но если его нагреть или добавить яркий солнечный свет, реакция способна привести к взрыву.
Реакция хлора на воду следующая: образуется соляная и хлорноватистая кислота. Если в хлор внести фосфор, то последний загорится, в результате чего образуется трех,- и пятихлористый фосфор.
Чтобы получить хлор, необходимо осуществить электролиз концентрированных водных растворов NaCl. Со стороны угольного анода начнет выделяться хлор, а на катоде – водород. Используя хлор, получают хлористый водород и соляную кислоту, которая применяется с целью отбеливания бумаги и тканей и, если требуется обеззаразить питьевую воду.
Галогенные соединения с бромом имеют более низкую химическую активность, нежели с хлором. Бром с водородом соединяются лишь в условиях нагревания. Для получения брома необходимо окислить HBr. В промышленных условиях используются бромиды и хлористый раствор. На территории России основной источник брома – подземные буровые воды и насыщенные растворы определенных соляных озер.
У йода еще меньший показатель химической активности, которую имеют другие галогенные соединения. Несмотря на меньшую активность, данный элемент также способен вступать в реакцию со многими неметаллами в обычных условиях, в результате чего образуются соли (если обратить внимание, то слово «галоген» исходит от слов «рождение соли»).
Для реакции йода с водородом требуется довольно сильное нагревание. Сама реакция неполная, так как жидкий водород начинает разлагаться.
Сравнивая галогенные соединения, отмечается, что их активность становится меньше от фтора к астату. Особенность галогенов в том, что они вступают в реакцию со многими простыми веществами. В случае с металлами наблюдается быстрая реакция, при которой выделяется большое количество тепла.
Особенности добычи и использования галогенов
Добыча натрия
В естественных условиях галогены – анионы, поэтому для получения свободных галогенов применяется метод окисления электролизом или с использованием окислителей. К примеру, чтобы получить хлор, необходимо сделать гидролиз раствора поваренной соли. Галогенные соединения используются во многих отраслях:
- Фтор. Несмотря на большую реактивность, данный химический элемент находит частое применение в промышленности. К примеру, фтор – ключевой элемент тефлона и прочих фторполимеров. Также в виде органических химических веществ представим хлорфторуглероды, ранее используемые как хладагенты и пропелленты в аэрозолях. Впоследствии их прекратили применять, так как была вероятность, что они воздействуют на окружающую среду. Фтор часто встречается в составе зубной пасты, направленный на сохранение целостности зубов. Также данный галоген можно застать в глине, где он актуален для производства керамики;
- Хлор. Наиболее частое использование хлора – дезинфекция питьевой воды и бассейнов. А такое соединение, как гипохлорит натрия, – основной компонент отбеливателя. Промышленные структуры и лаборатории не обходятся без применения соляной кислоты. В состав поливинилхлорида также входит фтор, как и в другие полимеры, при помощи которых осуществляется изоляция труб, проводки и прочих коммуникаций. Нашлось хлору применение и в фармацевтике, где на его основе производятся лекарства, при помощи которых лечатся инфекции, аллергии и диабет. Как было отмечено выше, хлор хорошо дезинфицирует, поэтому с его помощью стерилизуется больничное оборудование;
- Бром. Главная особенность данного химического элемента в том, что он негорюч. По этой причине он успешно используется для подавления горения. Бром в составе с другими элементами в одно время шел для производства специальных средств для огорода, благодаря которым гибли все бактерии. Но со временем средство запретили с предлогом, что последнее оказывает негативное воздействие на озоновый слой планеты. Также бром актуален в таких сферах: производство бензина, изготовление фотопленки, огнетушителей и некоторых лекарств;
- Йод. Важный химический элемент, от которого зависит правильное функционирование щитовидной железы. Из-за нехватки йода в организме последняя может даже начать увеличиваться в размерах. Йод себя отлично зарекомендовал как антисептическое средство. Йод встречается в растворах, при помощи которых очищают раны;
- Астат. Данный галоген является не только редкоземельным, но и радиоактивным, по этой причине не находит особенного применения.
Галогены и их физические свойства
Внешний вид фтора
Наличие тех или иных химических и физических свойств напрямую зависит от строения атома элемента. По большей части, у всех галогенов схожие свойства, но все же имеются определенные особенности:
- Фтор. Элемент в виде светло-зеленого газа с ядовитыми свойствами;
- Хлор. Желто-зеленый газ, также ядовитый, с резким, удушливым и неприятным запахом. Элемент способен легко растворяться в воде, из-за чего образуется хлорная вода;
- Бром. Выступает в качестве единственного жидкого неметалла. Это тяжелый элемент, выполненный в красно-буром цвете. Если поместить бром в какой-либо сосуд, стенки последнего окрасятся в красно-бурый цвет, выделяемый с парами галогена. Запах брома тяжелый и неприятный. Для хранения брома используются специальные склянки, имеющие притертые пробки и колпаки. Важно заметить, что последние не должны быть сделаны из резины, так как элемент способен легко разъесть этот материал;
- Йод. Темно-серое кристаллическое вещество, в парах имеющее фиолетовый цвет. Обычные условия не дают возможность привести йод в состояние плавления, а тем более кипения, так как даже слабое нагревание элемента приводит к его возгонке: когда он из твердого переходит в газообразное состояние. Этим свойством обладает не только йод, но и некоторые другие вещества. Это свойство пригодилось при очистке веществ от примесей. Йод – один из тех элементов, которые плохо растворяются в воде. Последняя получает светло-желтый цвет. Особенно хорошо йод способен растворяться в спирте, в результате чего начали делать 5-10% йодный раствор, называемый йодной настойкой.
Галогенные соединения и их роль в организме человека
При выборе зубной пасты многие обращают внимание на состав: есть ли в нем фтор. Данный компонент добавляется не просто так, ведь именно он способствует построению зубной эмали и костей, а также способен сделать зубы более стойкими к кариесу. Процессы обмена веществ также не обходятся без помощи фтора.
Йод содержится в продуктах питания
В организме человека немаловажное значение играет также хлор, активно участвующий в сохранении водно-солевого баланса, а также поддерживающий осмотическое давление. Благодаря хлору, эффективнее функционирует обмен веществ, построение тканей. Лучшему пищеварению способствует именно соляная кислота, без которой невозможно было бы переваривать пищу.
Хлор обязателен для человеческого организма и должен поступать в него в определенных количествах. Если пренебрегать нормой поступления элемента в организм, можно столкнуться с отеками, головными болями и прочими неприятными ощущениями.
Бром в небольших количествах находится в мозге, почках, крови и печени. В медицине бром – отличное средство успокоительного типа. Однако его необходимо давать в строгих пропорциях, так как последствия у передозировки не лучшие: угнетенное состояние нервной системы.
Йод строго необходим щитовидной железе, помогая последней активно бороться с поступающими в организм бактериями. Если в организме человека недостаточно йода, может начаться заболевание щитовидной железы.
В качестве вывода отметим, что галогены необходимы не только для реализации многих повседневных вещей, но и для эффективного функционирования нашего организма. Данные химические элементы имеют определенные особенности, которые находят свое применение в различных отраслях человеческой жизнедеятельности.
Видео
Оцените статью:elquanta.ru
Что такое галогены в химии? :: SYL.ru
Поговорим о том, что такое галогены. Они находятся в седьмой группе (главной подгруппе) таблицы Менделеева. В переводе с греческого языка "галоген" означает "рождающий соль". В статье пойдет речь о том, что собой представляет химический галоген, какие вещества объединены под этим термином, каковы их свойства и особенности получения.
Особенности
Рассуждая о том, что такое галогены, отметим специфику строения их атомов. У всех элементов на внешнем энергетическом уровне располагается по семь электронов, причем один из них является неспаренным (свободным). Поэтому ярко выражены окислительные свойства галогенов, то есть присоединение одного электрона во время взаимодействия с различными веществами, что приводит к полному завершению внешнего энергетического уровня, образованию устойчивых конфигураций галогенидов. С металлами они образуют прочную связь ионного характера.
Представители галогенов
К ним относятся следующие элементы: фтор, хлор, бром, йод. Формальное отношение к ним имеют астат и теннесин. Для того чтобы понять, что такое галогены, необходимо отметить, что у хлора, брома, йода есть свободная орбиталь. Именно она объясняет различные степени окисления у данных элементов. Например, хлор имеет следующие величины: -1, +1,+3, +5, +7. При сообщении атому хлора дополнительной энергии, происходит постепенный переход электронов, который и объясняет изменения в степенях окисления. Среди самых устойчивых конфигураций хлора выделяют его соединения, в которых проявляется степень окисления -1, а также +7.
Нахождение в природе
Особенности строения объясняют их распространенность в природе. Соединения галогенов в природе представлены в виде галогенидов, хорошо растворимых в воде. С увеличением атомного радиуса галогена происходит снижение их количественного содержания в земной коре. Например, некоторые соединения брома, хлора, фтора используют в промышленных объемах.
В качестве основного соединения фтора, представленного в природе, можно отметить фторид кальция (флюорит).
Особенности получения
Для того чтобы понять, что такое галогены, необходимо выяснить способы их получения. Основным вариантом выделения чистых галогенов из солей является электролиз расплавов солей. Например, при воздействии на хлорид натрия постоянного электрического тока в качестве продуктов реакции можно рассматривать не только газообразный хлор, но и металлический натрий. На катоде происходит восстановление металла, а галоген образуется на аноде. Для получения брома используют морскую воду, проводя электролиз этого раствора.
Физические свойства
Остановимся на физических свойствах представителей седьмой группы главной подгруппы. Фтор при обычных условиях является газообразным веществом, имеющим светло-желтый цвет, резкий и раздражающий запах. Газообразен и желто-зеленый хлор, имеющий резкое удушливое амбре. Бром является коричневой тяжелой жидкостью. Из всех галогенов только йод - кристаллическое вещество фиолетового цвета.
Самым сильным окислителем является фтор. В группе способность присоединять электрон во время химической реакции постепенно снижается от фтора к астату. Причина ослабления этого свойства заключается в увеличении атомного радиуса.
Особенности химических свойств
Фтор, являясь самым сильным окислителем, способен вступать без дополнительного нагревания во взаимодействие практически со всеми неметаллами. Процесс сопровождается выделением большого количества теплоты. С металлами процесс характеризуется самовоспламенением фтора.
Поскольку данный галоген отличается высокой химической активностью, он способен взаимодействовать при облучении с благородными газами.
Фтор вступает во взаимодействие и со сложными веществами. У брома активность существенно ниже. В основном он используется в органической химии для проведения качественных реакций на непредельные соединения.
Йод вступает во взаимодействие с металлами только при нагревании, причем процесс характеризуется поглощением энергии (экзотермическая реакция).
Особенности использования
Каково значение галогенов? Для того чтобы ответить на этот вопрос, рассмотрим основные области их применения. Например, природный минерал криолит, являющийся соединением алюминия, фтора, натрия, используется в качестве добавки в зубную пасту, способствует предотвращению кариеса.
Хлор в больших количествах применяют в производстве соляной кислоты. Кроме того, этот галоген востребован в изготовлении пластических масс, растворителей, красителей, каучуков, синтетических волокон. Большое количество хлорсодержащих соединений применяется для эффективной борьбы с различными вредителями сельскохозяйственных культур. Хлор, а также его соединения необходимы и для процесса отбеливания хлопчатобумажных и льняных тканей, бумаги, обеззараживания питьевой воды. Бром и йод используют в химической и фармацевтической промышленности.
В последнее время вместо хлора для очистки питьевой воды стали использовать озон.
Биологическое действие
Высокая реакционная способность галогенов объясняет тот факт, что все эти соединения являются ядами, имеющими удушающее действие, способными поражать органические ткани. Несмотря на такие характеристики, данные элементы необходимы для процессов жизнедеятельности человеческого организма.
Например, фтор участвует в обменных процессах в нервных клетках, мышцах, железах. В быту все чаще встречается тефлоновая посуда, одним из компонентов которой является именно фтор.
Хлор способствует росту волос, стимулирует обменные процессы, дает организму силы и бодрость. Максимальное количество его в виде хлорида натрия входит в состав плазмы крови. Среди соединений данного элемента особый интерес с биологической точки зрения представляет соляная кислота.
Именно она является основой желудочного сока, участвует в процессах расщепления пищи. Для того чтобы организм функционировал нормально, в сутки человек должен употреблять не меньше двадцати граммов поваренной соли.
Все галогены необходимы человеку для жизнедеятельности, а также используются им в разных сферах деятельности.
www.syl.ru














